|
|


Campaña contra las pruebas de toxicidad
en animales de la Unión Europea
Infórmate y apoya esta campaña
para evitar que millones de
animales sufran y mueran
[ver otras campañas solidarias]
Envía esta página a otras personas,
¡corre la voz! Haz
clic aquí
A pesar del compromiso de reducir la experimentación en animales en un 50% para el año 2001, la nueva política que está impulsando la Unión Europea relativa a productos químicos podría costarle la vida a unos 10 millones de animales y podría permitir que se liberasen en el ambiente sustancias peligrosas.
La propuesta de probar en animales las sustancias químicas existentes y habitualmente usadas, representaría el mayor programa de pruebas de toxicidad en la historia de Europa. Si no damos una respuesta inmediata, este programa podría someter a tests de toxicidad a unos 500.000 animales al año, que causarían efectos secundarios como hemorragias internas, convulsiones, ataques epilépticos, parálisis y finalmente la muerte.
La comunidad científica e incluso la industria química, han criticado duramente la utilización de animales en estas pruebas. Idear e implementar una política adecuada de sustancias químicas en Europa es una oportunidad para que todas las partes interesadas trabajen juntas (ecologistas, asociaciones de consumidores, defensores de los animales, compañías y organismos reguladores. El objetivo de dicha política (identificar y ejercer un control efectivo sobre las sustancias dañinas), es de interés común.
Necesitamos tu ayuda urgente para evitar que los animales sean sujetos de pruebas terriblemente crueles, inútiles e ineficaces, y para apoyar el desarrollo de una política europea en materia de químicos que proteja de manera efectiva la salud y bienestar de todos los consumidores, los animales y el medio ambiente. Por favor, lee la información que aparece a continuación, participa en las acciones que se piden y difúndela lo más posible entre tus conocidos.
Protección medioambiental
Teniendo en cuenta que las sustancias que se pretenden probar por el programa de químicos de la UE han sido ampliamente utilizadas desde hace muchos años, los organismos oficiales deberían tener datos bastante precisos acerca de las mismas, en lo que concierne a sus propiedades, toxicidad y efectos ambientales. Dicho de otra forma, ya deberíamos saber por experiencia qué sustancias químicas son tóxicas o peligrosas, así como aquellas que son persistentes (resistentes a biodegradación) o bioacumulativas (capaces de concentrarse en los tejidos corporales).
Asociación Americana de Ciencia y Política Pública: "Las pruebas en animales funcionan esencialmente como un mecanismo para evitar demandas por responsabilidad, pues los dudosos resultados generan a su vez interminables estudios que sólo llevan a la inacción. Los resultados ambiguos y las interpretaciones subjetivas de los estudios con animales, han creado una atmósfera que conduce a la arbitrariedad y a tomar decisiones caprichosas, permitiendo que los organismos reguladores estén sometidos a las presiones de los intereses del mercado en asuntos concernientes a la salud pública".
Los Tests
Los expertos estiman que la nueva política europea de sustancia químicas puede llegar a matar hasta 10 millones de animales en 20 años. Aunque la Comisión Europea debe todavía publicar los detalles exactos del protocolo de tests propuesto, probablemente conlleve estudios de toxicidad (envenenamientos) a corto y largo plazo, en especies como ratas, ratones, cobayas, conejos, pájaros, peces, invertebrados y perros. Una "batería" de pruebas habitual, incluye los siguientes tipos de estudios:
Toxicidad aguda
Las pruebas de toxicidad aguda se llevan a cabo para determinar el potencial para causar lesiones o la muerte de un producto químico, tras una exposición breve al mismo (normalmente hasta 24 horas). Los estudios más comunes de toxicidad aguda (el test LD-50 y sus derivados) han sido reconocidos ampliamente como no científicos, imprecisos y extremadamente crueles. Estas pruebas requieren el uso de roedores u otros animales, y su terminación significa bien la muerte o bien un alto grado de envenenamiento para la mitad de los animales utilizados. La cantidad de sustancia de prueba requerida para inducir esta respuesta tóxica se usa para calcular la dosis letal predecible al 50% (LD-50).
Se expone a los animales a pruebas químicas a través de los siguientes métodos:
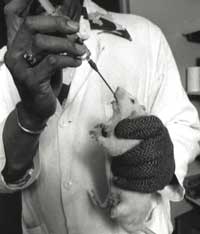
- Oral: Los químicos se introducen directamente en el estómago del animal forzándole a ingerirlos a través de una jeringa o un tubo, o a través de la comida. Las pruebas de toxicidad oral aguda causan un dolor y estrés extremos a los animales implicados, que pueden sufrir convulsiones, dolor abdominal severo, ataques epilépticos, diarrea, hemorragia en ojos, boca o genitales, parálisis, y finalmente la muerte.
- Inhalación: Se fuerza a los animales a respirar vapores químicos durante un periodo de tiempo fijo. Esto se lleva a cabo, bien colocando a los animales en una cámara de inhalación hacia la que se bombea el químico, o inmovilizándolos y colocándoles un aparato de inhalación sobre la boca. Los estudios de inhalación forzada son altamente estresantes para los individuos implicados, especialmente aquellos que son retenidos durante largos periodos de tiempo. Efectos como hemorragia nasal, respiración fatigada, convulsiones, coma o la muerte son habituales.
- Piel: En los estudios dérmicos de toxicidad, se afeita el lomo de conejos, cobayas o ratas, y se les aplica una sustancia de prueba, para medir el grado de penetración de una sustancia a través de la piel. Los experimentos pueden durar periodos de hasta dos semanas, para determinar el grado de penetración necesario en la piel para matar al animal.
Dosis de toxicidad repetida
Los estudios de dosis de toxicidad repetida requieren la exposición de animales a dosis suaves y repetidas de químicos, en periodos de 14 a 90 días. El propósito de estas pruebas es evaluar los efectos de la exposición crónica de bajo nivel a químicos, en órganos como el hígado, los riñones, los pulmones, el corazón o el sistema nervioso. El protocolo de prueba recomienda las exposiciones por vía oral, dérmica o por inhalación. Estas pruebas son extremadamente estresantes, ya que los animales son expuestos repetidamente a procedimientos tales como la alimentación forzada.
Toxicidad reproductiva
Los estudios de toxicidad en la reproducción examinan los efectos de determinadas sustancias en la fertilidad y órganos reproductivos. Los protocolos requieren estudios de dosis repetidas de entre 28 y 90 días, durante los cuales se examina a los animales en su comportamiento sexual, producción de esperma o huevos y fertilización, actividad in utero y desarrollo postnatal. Al final de cada pruebas, a menudo se amputan los genitales u órganos reproductivos para su posterior estudio.
Toxicidad de desarrollo
Las pruebas de toxicidad de desarrollo o teratogenicidad, se llevan a cabo para determinar el potencial de una sustancia química para afectar el desarrollo de las crías durante periodos críticos de crecimiento y desarrollo. Estas pruebas normalmente implican estudios de dosis repetidas en periodos de entre 28 y 90 días sobre roedores preñados, y se pueden combinar con estudios de toxicidad reproductiva como los descritos arriba. Efectos habituales de este tipo de envenenamiento incluye anomalías en el desarrollo y deformidades físicas, toxicidad materna, abortos y muerte de los embriones.
Además de estas pruebas, que componen el protocolo SIDS (Conjunto de Datos de Información para la Investigación, en sus siglas en inglés) de la OCDE, otros estudios habituales en animales evalúan el potencial de sustancias químicas para dañar los ojos (irritación ocular), el sistema nervioso (neurotoxicidad), causar cancer (carcinogenicidad) y afección al sistema hormonal (endocrino).
Virtualmente, todos los estudios de toxicidad generan en los animales implicados grados extremos de ansiedad y dolor. Además, todos los animales envueltos en este tipo de pruebas, o bien morirán a causa del experimento, o se les matará en un punto determinado para llevar a cabo un examen post-mortem de los efectos estudiados. Como ilustran los ejemplos anteriores, el programa de estudios químicos propuesto significa muerte y sufrimiento para todos y cada uno de los animales implicados. Una acusación particularmente grave que se puede hacer al programa propuesta por la UE, es que 20 años y 10 millones de animales muertos más tarde, los legisladores no serán capaces de proteger a los consumidores o al ambiente debido a las limitaciones inherentes a las pruebas de toxicidad basadas en animales.
Hechos científicos
Dr. Joshua Lederberg, Nobel Laureado en Medicina: "Es sencillamente imposible, con todos los animales que hay en el mundo, manipular las sustancias químicas como lo hacemos ahora, y llegar a conclusiones creíbles sobre los riesgos para la salud humana".
Para que el programa de pruebas químicas propuesto por la UE tuviera alguna credibilidad científica, la metodología utilizada debería ser capaz de garantizar una validez científica, relevante biológicamente, fiable y cuyos resultados puedan reproducirse.
Hay un corpus considerable de evidencia que documenta la incapacidad de las pruebas de toxicidad basadas en animales para predecir con precisión las reacciones humanas a los productos químicos. Estos errores no resultan sorprendentes, dadas las múltiples diferencias que existen entre especies a nivel anatómico, fisiológico, bioquímico y metabólico. Estas variables hacen la extrapolación de pruebas entre especies un ejercicio enormemente incierto.
Los siguientes ejemplos ilustran algunos estudios clave de toxicidad basados en animales:
- En el Estudio de Evaluación Multicentro de Citotoxicidad In Vitro (MEIC, en sus siglas en inglés), se examinaron datos de la prueba LD-50 sobre ratas y ratones para 50 químicos, y se encontró que estos tests eran capaces de predecir toxididad en personas sólo a un nivel de precisión del 65%. En realidad, los científicos participantes en una conferencia internacional reciente sobre alternativas a las pruebas de toxicidad aguda, que tuvo lugar en Washington DC, afirmaron que no es ni siquiera seguro que la prueba LD-50 pueda predecir la letalidad en las propias ratas. Como contraste, una batería de pruebas no basadas en animales, que utilizaba células humanas, fue capaz de predecir la toxicidad en personas con una precisión del 84%.
- Al contrario que con los humanos, los roedores no poseen el acto reflejo de vomitar. Por tanto, no son capaces de expulsar sustancias nocivas del cuerpo, con lo que su nivel de exposición a sustancias químicas se incrementa proporcionalmente, lo que hace la extrapolación a seres humanos altamente cuestionable.
- Los roedores sólo viven de dos a tres años, la duración de la vida de los seres humanos es de 75 años en adelante. Esto es muy significativo, cuando se estudian los efectos de la toxicidad a largo plazo. Por ejemplo, las ratas son más vulnerables al cancer que las personas, las cuales, debido a su mayor longevidad, han desarrollado comparativamente más defensas contra el cáncer espontáneo.
- Además de las diferencias entre las distintas especies animales, también hay diferencias significativas entre sub-especies y en diferentes razas de la misma especie. Por ejemplo, la sustancia n,2fluorocenilacetamida causa causa cáncer de vejiga en ratas macho y hembra del tipo Slonaker, cancer de hígado en ratas de tipo Wistar y cancer de pecho en ratas hembras de este último género, también cancer intestinal en ratas macho y hembra del tipo Piebald. El Etil-carbamato genera una elevada incidencia de cáncer de determinadas razas de ratones, pero no en otras. Se ha averiguado que el cloroformo causa cáncer de hígado en las hembras de determinadas razas, pero no en los machos.
- También ha habido numerosos casos donde las pruebas de toxicidad basadas en animales no han sido capaces de predecir taras de nacimiento en seres humanos. Por ejemplo, una serie de desinfectantes comercializados en Italia con los nombres Mipaphox, Trichlorphan y Diptorex, causaban daños al sistema nervioso humano de otros animales, a pesar de que en las pruebas realizadas con ratones se les administraban dosis de hasta 1.500 mg/kg sin efectos negativos aparentes.
- Las deficiencias de los experimentos realizados en animales son también evidentes teniendo en cuenta los estudios realizados sobre carcinogenicidad. Por ejemplo, el arsénico no estaba clasificado como carcinógeno según los estudios con animales, pero posteriormente se encontró que causaba altos niveles de cáncer de pulmón en trabajadores de fundiciones expuestos a arsénico en el aire. De forma similar, el nexo causal entre el benceno y la leucemia humana se estableció en 1928, no obstante, 14 estudios posteriores en animales no pudieron demostrar este efecto.
Más ejemplos sobre diferencias inter-especies en la respuesta a sustancias químicas:
- 1)N,2-fluorenilacetamida:
- a) causante de cáncer de vejiga en ratas Slonaker macho y hembra
- b) causante de cáncer de hígado en ratas Wistar macho y cancer de mama en ratas Wistar hembra
- c) causante de cáncer intestinal en ratas Piebald macho y hembra
- 2) N-nitrosodietilamina:
- a)causante de tumores en el hígado en ratas de Noruega (BD II), ratas de cola blanca, pollos, cobayas, ratones NMRI y hamsters dorados de Siria, en dosis que para cada especie variaban en millares de veces.
-
3) Etil carbamato:
-
a) causante de altas incidencias de cáncer en determinadas razas de ratones pero no en la raza X/Gf.
-
4) Dimetil-benzo-alfa-antraceno:
- a) causante de linfomas en ratones suizos
- b) causante de adenomas bronquiales en la raza de ratones Fuerte A
- c) causante de hepatomas (cáncer de hígado) en ratones hembra de otras especies.
-
5) Benzidina:
-
a) causante de cáncer de vejiga en humanos
- b) causante de tumores en el nervio acústico, el intestino y el hígado en ratones
-
6) Carbontetraclorido (CC1):
-
a) causante de tumores de hígado en ratones
- b) produce cirrosis en el hígado de ratas
-
7) Cloroformo (CHC1) (ver arriba):
-
a) produce tumores en el hígado en hembras de varias razas pero no en los machos.
-
8) DDT:
-
a) causante de tumores en el hígado de ratones pero no en ratas o hamsters
-
9) Sacarina sódica (edulcorante artificial):
-
a) causante de cáncer de vejiga sólo en ratas macho
- b) monos machos y hembras, hamster y ratones no se vieron afectados incluso con dosis elevadas.
- c) Estudios epidemiológicos no pudieron encontrar evidencia de cáncer de vejiga en humanos.
-
10) Arsénico:
-
a) carcinógeno en humanos
- b) no carcinógeno en roedores
-
11) Benzidina y 2-naptilamina:
-
a) causante de cáncer de vejiga en humanos y perros
- b) causante de tumores de hígado y mamas de ratas
- c) causante en gran medida de tumores en el hígado de ratones y hamsters.
-
12) Productos de fibra de vidrio:
-
a) Experimientos en ratas, cobayas, conejos y primates en los años 50, no producían daño en los pulmones cuando se forzaba a los animales a inhalar fibra de vidrio. Un análisis posterior en los años 80 reveló que ni los hamsters, ni las cobayas ni los ratones ni los primates expuestos a fibra de vidrio, lana de vidrio o lana mineral sufrían tumores en los pulmones después de largas sesiones de inhalación.
- b) En 1991, la Administración de Salud y Seguridad Ocupacional de Estados Unidos decidió que los productos con fibra de vidrio debían etiquetarse como generadores de riesgo de cáncer porque, contrariamente a los experimentos con animales, estudios en trabajadores industriales mostraron un riesgo incremental de cancer de pulmón.
Las Alternativas
A continuación mostraremos un breve resumen de los métodos alternativos que pueden potencialmente ser utilizados como sustitutos a las pruebas con animales en determinadas pruebas de toxicidad:
- Toxicidad oral aguda.
Existe una considerable cantidad de investigación dirigida al desarrollo y validación de métodos alternativos a las pruebas de toxicidad aguda. Partiendo de la premisa de que la acción de los productos químicos que producen la toxicidad tiene lugar a nivel celular, se han desarrollado numerosas pruebas de toxicidad celular in vitro para su uso como filtros previos y como sustitutos potenciales de las pruebas LD-50. Muchas de estas pruebas hacen uso de varios tipos de tejidos (como células madre, del hígado, del riñón, etc) para estimar los efectos de un químico sobre diferentes sistemas de órganos.
En la actualidad, se cree que una aproximación por niveles combinando modelos por ordenador de relaciones cuantitativas estructura-actividad (QSAR), junto con una bateria de cuatro o más pruebas de toxicidad celular in vitro, es el sustituto más prometedor para el uso de animales en las pruebas de toxicidad aguda. Tal aproximación ya ha demostrado ser capaz de predecir toxicidad en humanos con un impresionante porcentaje de precisión del 84%.
-
Absorción dérmica. La absorción de sustancias químicias a través de la piel puede ahora modelizarse in vitro por medio de células humanas extraídas de cadáveres y determinadas con técnicas de difusión celular in vitro. Un método particular de prueba de absorción dérmica in vitro ha sido recientemente aceptado como sustituto para los estudios de penetración dérmica basados en animales.
-
Corrosión de la piel.Los productos químicos corrosivos pueden identificarse de manera fiable utlizando métodos in vitro como el procedimiento de Resistencia Eléctrica Transcutánea (TER), el test EPISKIN de piel humana reconstituida y el CORROSITEX. Estos métodos han sido todos ellos aceptados y validados por organismos reguladores como totalmente válidos para sustituir el uso de animales en pruebas de corrosión cutánea, por tanto, no es necesario seguir utilizando animales en este tipo de estudios.
-
Toxicidad en Dosis Repetidas.Los métodos alternativos propuestos como sustitutos a las pruebas en animales en los estudios de toxicidad en dosis repetidas incluyen cultivos in vitro de tejidos de diferentes órganos. Por ejemplo, un cultivo de células de hígado humano puede ser expuesto a dosis bajas de productos químicos en intervalos de tiempo variable, para poder estudiar no sólo los efectos patógenos de una sustancia, sino también su metabolismo, así como para identificar cualquier metabolito potencialmente dañino que se produzca en este proceso. De forma similar, se han establecido cultivos estables de células humanas del riñón, sistema nervioso, sistema inmunitario, sistema reproductivo y otros órganos o sistemas esenciales. Una batería de cada uno de estos cultivos adicional al modelado matemático o por ordenador, puede proporcionar un sustituto válido a los animales en los estudios de toxicidad en dosis repetidas.
-
Genotoxicidad. Las alternativas a los experimientos con animales en estudios de genotoxicidad incluyen el test Ames (con bacterias), el método CHO que utiliza células en probetas, así como el reciente test in vitro micronúcleo. Algunas de estas pruebas son también útiles para predecir si un químico puede causar cáncer.
El Comité de Mutagenicidad de Químicos del Reino Unido, afirmó que el uso de pruebas in vitro "...si se guían por protocolos exhaustivos, deberían tener como resultado la detección de, excepto una pequeña parte, todos los químicos con potencial genotóxico. Por otra parte, si la batería de pruebas se ha ampliado para incluir ensayos de mutación de genes en células de mamíferos, se considera entonces que el número de mutágenos que pueden perderse es lo suficientemente bajo para no requerir el uso de pruebas in vivo para propósitos de investigación".
En otras palabras, productos químicos que dan positivo en estos ensayos deberían aceptarse como perjudiciales y recibir la regulación correspondiente. No deberían seguir probándose sus efectos tóxicos carcinógenos o reproductivos/de desarrollo en animales.
-
Toxicidad en la reproducción.
Se pueden modelar in vitro varios aspectos de las funciones reproductivas masculinas y femeninas, y pueden mantenerse en cultivos varios componentes celulares de los distintos órganos reproductivos.Aunque ninguno de ellos se ha utilizado o validado como investigación rutinaria de toxicidad reproductiva, se cree que una batería de pruebas de este tipo podría ser capaz de servir como modelo para una gran proporción del ciclo reproductivo femenino y masculino.
-
Toxicidad en el desarrollo
En la actualidad se están validando diversas pruebas susceptibles de predecir qué sustancias químicas pueden causar defectos en el nacimiento u otro tipo de toxicidad en el desarrollo. Algunas de estas pruebas utilizan embriones animales en estados primarios (como el FETAX), pero el test de células madre embrionarias, que está actualmente siendo validado en Europa, utiliza cultivos de células en probeta. La precisión general de estas pruebas en predicción de potencial teratogénico ha sido evaludada en un 83%.
De manera más general, las siguientes aproximaciones basadas en modelos de ordenador se han mostrado muy prometedoras en la contribución a la sustitución de animales en pruebas de toxicidad:
-
Relaciones de Estructura-Actividad basadas en ordenador. Las relaciones Estructura-Actividad (SAR) utilizan ordenadores para predecir efectos biológicos adversos de sustancias químicas basándose en su estructura molecular, peso y carga electrónica. Los datos de las SAR pueden utilizarse para estimar si un producto químico determinado produce una respuesta biológica concreta, incluyendo toxicidad, sin recurrir a animales. Estos modelos han probado un porcentaje de precisión de entre el 85% y el 97% para predecir sensibilidad dérmica, teratogenicidad y carcinogenicidad para grupos relacionados de sustancias químicas. Estos modelos por ordenador pueden utilizarse para investigar químicos, pero no pueden operar como sustitutos por sí mismos. Por lo tanto, se usan en combinación con otras metodologías.
- Modelos Matemáticos por Ordenador.
Ahora es posible utilizar ordenadores para el modelado de sistemas biológicos vivos, como los sistemas circulatorio y respiratorio humanos, con parámetros numéricos. Por ejemplo, los modelos fisiológicos bio-cinéticos (PBBK) utilizan ordenadores para estudiar la absorción, distribución, metabolismo y excreción de químicos por el cuerpo. También pueden utilizarse para determinar la relación entre una dosis química y un efecto metabólico particular. Uno de estos modelos, el ED01, estudia la producción de tumores en respuesta a la exposición química. Es capaz de detectar una actividad de crecimiento de un tumor de un 1%, y con dosis de producto químico mucho más bajas que las que se suelen utilizar en las pruebas con roedores.
Obstáculos para la aceptación de métodos alternativos
A pesar de los considerables esfuerzos que se están llevando a cabo para desarrollar alternativas sustitutorias a las habituales pruebas con animales, se ha progresado relativamente poco a la hora de obtener aceptación de estos tests por parte de los organismos reguladores. La resistencia al cambio ha resultado ser significativa, lo que quiere decir que los científicos y los reguladores tenderán a usar las técnicas con las que están familiarizados y que ellos comprenden. Se ha identificado una serie de obstáculos que están impidiendo el progreso en la aceptación de métodos alternativos sin animales:
-
Obstáculo regulador: Los reguladores estatales llevan el peso de la responsabilidad para la interpretación de datos seguros. Como tales, el miedo al cambio, particularmente motivado por la aparición de nuevas metodologías, es una actitud común entre estos reguladores, y un obstáculo importante para la aceptación de métodos sin animales.
-
Obstáculo legislativo: cualquier método alternativo, si quiere tener un impacto importante sobre el no uso de animales con fines experimentales, necesitará estar incluido dentro de alguna normativa oficial de pruebas. La normativa de pruebas de la Organización para la Cooperación y el Desarrollo Económico (OCDE) es un estándar mundialmente aceptado, del que derivan muchas otras normativas, y constituye por tanto un paso crucial en la aceptación de métodos alternativos sin animales.
En la actualidad, la normativa de pruebas de la OCDE y el protocolo SIDS (Conjunto de Datos de Información para la Investigación), requieren abrumadoramente el uso de pruebas que implican el uso animales. Aunque la OCDE tiene por norma aceptar sólo métdos alternativos validados científicamente, debe observarse que, a pesar de que los largos y rigurosos procesos de validación a que son sometidos los métodos sin animales, ¡de los tests con animales actualmente utilizados, muy pocos o ninguno han pasado por algún proceso de validación!
Este doble rasero es ciertamente digno de tener en cuenta. Mientras que, por un lado, la OCDE exige unos procesos largos y extremadamente severos para la validación de métodos sin animales, por otra parte acepta rápidamente pruebas con animales que nunca han sido validados científicamente de alguna manera que remotamente se aproxime a los procesos que se requieren para aprobar pruebas sin animales.
- Obstáculo de validación: la validación es un proceso que establece la fiabilidad y relevancia de un metodo de pruebas. La fiabilidad es la capacidad de reproducir los resultados en los mismos u otros laboratorios, y la relevancia es el ámbito para el cual un test es significativo y útil para un propósito determinado. La aceptación regulativa debe tener lugar cuando un método de prueba ha demostrado ser apropiado para la determinación de riesgos o daños con el objeto de salvaguardar la salud pública y ambiental.
Algunas personas han sugerido que el proceso de validación actual consume demasiado tiempo innecesariamente, y es en sí mismo uno de los factores principales que retrasa la introducción de métodos de prueba sin animales. Se trata de procesos que pueden durar incluso hasta 10 o más años. Además, durante la validación, las pruebas alternativas sin animales deben validarse precisamente frente a esas mismas pruebas en animales no validadas a las que pretenden sustituir. Teniendo en cuenta que uno de los principales argumentos contra la experimentación en animales es su falta de fiabilidad inherente, estas pruebas representan un punto de referencia tremendamente pobre para juzgar los métodos alternativos.
El camino a seguir
Puesto que la Comisión Europea debe asegurar que las metodologías de pruebas para su programa de estudios químicos sean biológicamente relevantes, precisas y repetibles. Para conseguirlo, está obligada a dar preferencia activa a las prometedoras pruebas sin animales, apoyar económicamente su validación y promover sin vacilaciones su aceptación por los organismos reguladores.
Una revisión de las políticas de químicos de la UE ofrecería una oportunidad única y apasionante para que la Comisión Europea revalore su enfoque actual sobre pruebas químicas y regulación. En lugar de fiarse de métodos caducos, no fiables y altamente criticados como los probados en animales. Ahora la Comisión tiene la posición para iniciar un nuevo programa basado en métodos más prácticos, eficientes, económicos y humanos. Un enfoque de este tipo no solamente salvaría la vida de incontables animales, sino que además beneficiaría a la protección medioambiental, y a la seguridad humana y del consumidor.
Recomendamos que se tengan en cuenta las siguientes indicaciones para el nuevo programa europeo de pruebas químicas:
- Obligatoriedad para todas las empresas y países de compartir públicamente sus datos, para hacer uso de la mayor cantidad posible de datos químicos existentes y evitar duplicaciones de pruebas. Las compañías químicas de todo el mundo ya poseen enormes cantidades de datos respecto a los productos que comercializan, muchos de los cuales nunca se hace públicos. Si se les obligara a hacerlo, muchos de los lapsos de datos que se observen para los químicos se rellenarían.
- Posponer el programa de pruebas propuesto para un mínimo de 3 años, con objeto de dar prioridad a la validación de nuevos y prometedores métodos in vitro. Para lograrlo, debe existir un compromiso firme de incrementar los fondos disponibles para el desarrollo de métodos alternativos (por ejemplo, a través del Centro Europeo para la Validación de Métodos Alternativos).
- Armonizar los procesos de validación internacionales para maximizar el uso de métodos alternativos válidos y evitar repetir estudios de validación.
- Priorizar la investigación en químicos a través de estudios rápidos sin animales (por ejemplo, a través estrategias graduales ya aceptadas por la OCDE).
- Tomando como base estos resultados, identificar los químicos que resultan ser más tóxicos.
- Los químicos que se clasifiquen como no tóxicos o de baja toxicidad a través de pruebas sin animales, pueden seguir siendo utilizados con precaución mientras se continuan experimentando.
- Las pruebas que se sigan haciendo deben asumir la incorporación de tests sin animales o esperar la validación final de los nuevos métodos alternativos, tutelados por la nueva iniciativa coordinada de la Comisión.
- Restringir, caducar o imponer una moratoria a la producción y utilización de aquellos químicos que resulten ser persistentes, bio-acumulativos o tóxicos. La mejor manera de proteger a las personas y al medio ambiente es reducir de forma activa su exposición a sustancias químicas potencialmente peligrosas.
Un enfoque de este tipo llevaría a la UE a modernizar sus estrategias de pruebas químicas y demostraría un claro compromiso de desarrollar métodos mucho más fiables y precisos. Esta perspectiva estaría también en consonancia con la directiva comunitaria 86/609, que prohíbe el uso de animales en experimentos donde existen métodos alternativos razonables y disponibles en la práctica. Los expertos en toxicología no animal coinciden en que esta perspectiva reforzaría la seguridad humana y ambiental ofreciendo resultados menos costosos y más rápidos, y de un valor científico equivalente o, a menudo, superior.
Qué puedes hacer
¡Tu apoyo es fundamental!
Los datos aquí expuestos han sido recopilados
y traducidos por la asociación española "Alternativa para la Liberación Animal" (ALA)
Fuente original: Campaña de BUAV y PETA
El portal redalternativa.com ha cedido este espacio gratuitamente a ALA para la difusión de esta campaña. Agradecemos la confianza depositada en nuestro proyecto.
|
|


 x
x